Bildnachweis: Universität Kyoto
Professor Koji Eto (Abteilung für klinische Anwendung) und sein Forscherteam haben in einem kürzlichen Versuch, die Blutplättchenherstellung mithilfe von Megakaryozyten aus iPS-Zellen zu erweitern, mithilfe von Computersimulationen und biologischen Tests neue Designmodifikationen für einen Turbinenbioreaktor entwickelt. für die großtechnische Waferproduktion in hoher Qualität. Die Studie ist veröffentlicht in Nachrichtentechnik.
Expandierbare immortalisierte Megakaryozyten-Vorläuferzelllinien aus iPS-Zellen (imMKCL) stellen eine erneuerbare Möglichkeit dar, große Mengen an Blutplättchen ex vivo für die Transfusion zu produzieren. Trotz der Generation von 100 Milliarden (1011) Aus iPS-Zellen gewonnene kompetente Blutplättchen unter Verwendung eines 10-L-Reservoirsystems durch vorherige Wiederherstellung einer turbulenten Strömung mit optimaler turbulenter Energie und Scherbeanspruchung. Für eine konstante Versorgung transfundierbarer Blutplättchen für Patienten mit Thrombozytopenie und anderen Blutplättchenerkrankungen ist eine echte Herstellung im industriellen Maßstab erforderlich.
Daher begann das Team diese Studie mit der Entwicklung eines 50-Liter-Einweg-Polyethylentanks der Good Manufacturing Practices (GMP) Klasse IV und eines neuen Motorreglers für eine kompetente Produktion von Wafern in noch größeren Maßstäben.
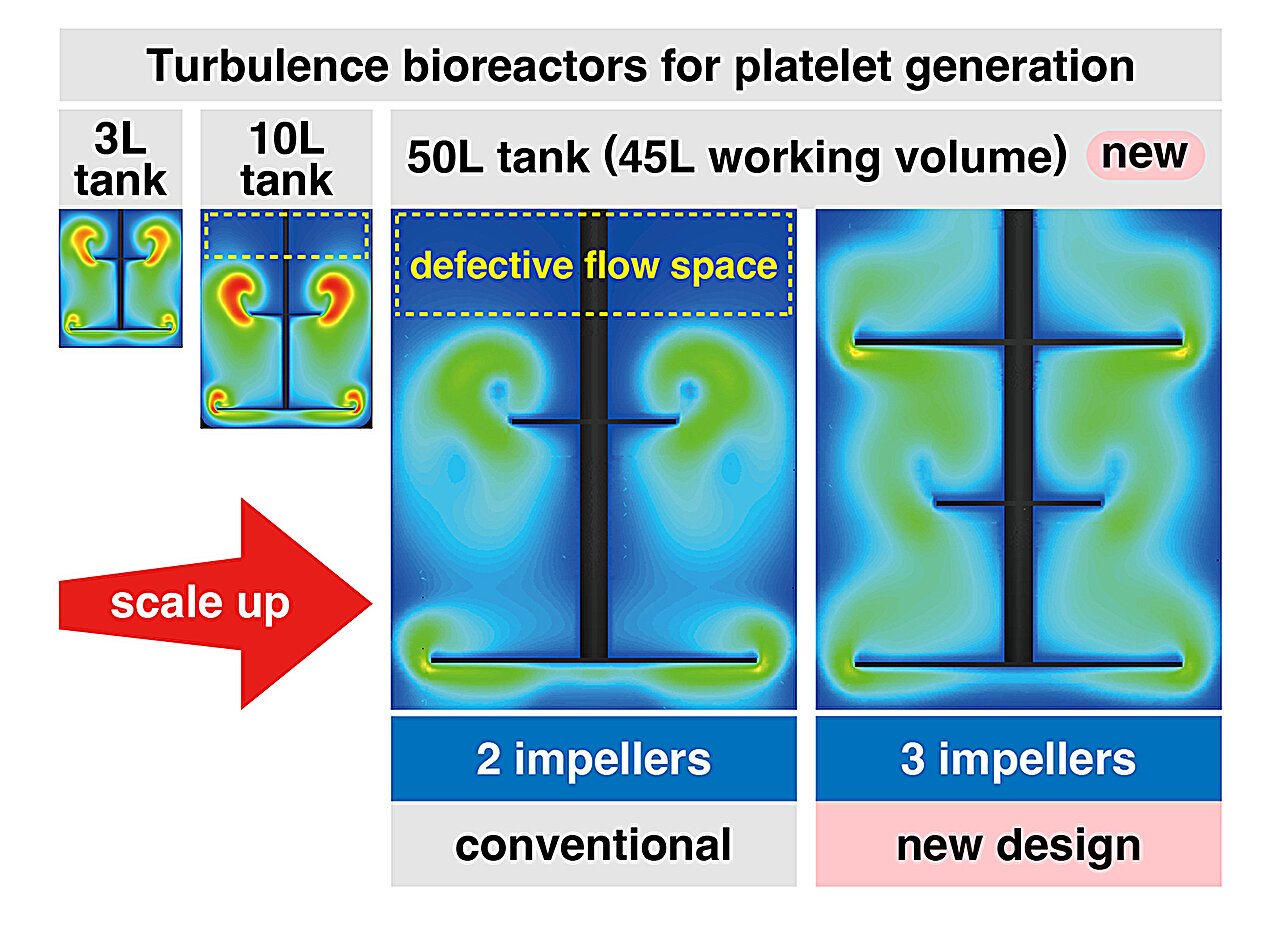
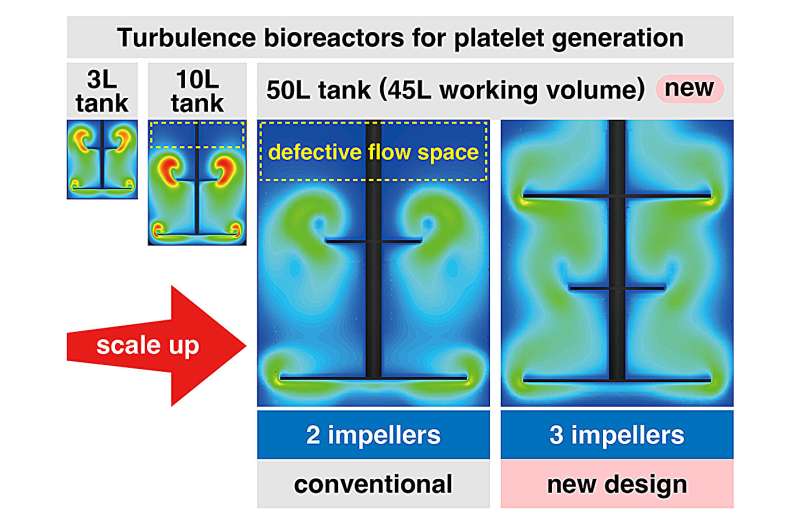
Durch Computersimulation der turbulenten Energie und Scherspannungen, die in diesen 50-Liter-Tanks erzeugt werden, mithilfe einer CFD-Analyse (Computational Fluid Dynamics) ermittelten die Forscher die optimale Bewegungsgeschwindigkeit für das größere System, um die Bedingungen in den zuvor untersuchten kleineren Tanks nachzuahmen. Bemerkenswerterweise zeigte der größere Tank durchweg geringere Wirkungsgrade als die kleineren getesteten Tanks (3 oder 10 l), obwohl die Geschwindigkeit optimiert wurde, um turbulente Energie und Scherspannung ähnlich einem Durchschnittswert zu erzeugen.
Darüber hinaus waren die im 50-L-Reservoir mit größerem Fassungsvermögen produzierten Blutplättchen nicht nur in geringerer Menge vorhanden, sondern sie waren auch qualitativ schlechter und zeigten bei der Untersuchung mittels Transmissionselektronenmikroskopie ultrastrukturelle Anomalien. Letztendlich zeigten sie eine schlechtere Leistung, als das Forschungsteam ihre Funktionen mithilfe von In-vitro- oder In-vivo-Tests (hämostatische und Kreislaufkinetik) nach der Transfusion in Mäuse bewertete.
Um biologische Einblicke in die Unfähigkeit zu erhalten, nach der Skalierung hochwertige Blutplättchen zu produzieren, sammelte das Forschungsteam imMKCL an den Tagen 3 und 5 der Blutplättchenproduktion bei unterschiedlichen Bewegungsgeschwindigkeiten und analysierte es mittels RNA-Sequenzierung. Die Hauptkomponentenanalyse ergab, dass die Kulturbedingungen die Expressionsprofile des imMKCL-Gens signifikant veränderten.
Während imMKCL unter optimalen Bedingungen (entsprechend kleineren Tankkulturen) Gene hochreguliert wurden, die mit Angiogenese, Zelladhäsion, Zytoskelett, Hypoxie, Blutplättchenfunktion und der Signalübertragung von TGF-β zusammenhängen, hochregulierte imMKCL bei übermäßiger Geschwindigkeit im Gegensatz dazu Gene, die mit Entzündungen und geschädigter Mitochondrienfunktion verbunden sind , was mit der Produktion weniger gesunder Blutplättchen vereinbar ist.
Als schließlich klar wurde, dass die Bedingungen für die Waferproduktion im großen Maßstab nicht ideal waren, ging das Forschungsteam zurück ans Zeichenbrett und führte zusätzliche CFD-Simulationen durch, um festzustellen, ob die turbulente Strömung nach der Skalierung nicht optimal geworden war. Insbesondere entdeckten sie durch diese Analyse, dass es im größten 50-Liter-Tank einen erheblichen Raum mit nicht optimierter turbulenter Strömung gibt.
Um diesen unerwünschten Raum (turbulentenfreies Volumen) zu minimieren, simulierte das Forschungsteam ein dreistufiges Turbinensystem und stellte fest, dass es bei fehlerhafter turbulenter Strömung das Volumen reduzieren sollte. Allerdings ist ein solches System derzeit nicht kommerziell erhältlich und so entwickelten Forscher ein neues Bioreaktorsystem, um eine gleichmäßigere Zellverteilung und turbulente Strömung zu gewährleisten. Es wurde eine kleine 3-Liter-Anlage gebaut, die erwartungsgemäß eine sehr effiziente Produktion hochwertiger Wafer zeigte.
Obwohl zusätzliche Arbeit erforderlich ist, um ein System in größerem Maßstab zu bauen und das neue Bioreaktordesign zu testen, geht das Forschungsteam davon aus, dass der Skalierungsprozess beim nächsten Mal reibungsloser ablaufen wird, da das neue Design nicht dieselben Einschränkungen aufweist.
Mehr Informationen:
Haruki Okamoto et al., Defekter Strömungsraum begrenzt die Skalierung von Turbulenzbioreaktoren zur Blutplättchenerzeugung, Nachrichtentechnik (2024). DOI: 10.1038/s44172-024-00219-y
Zur Verfügung gestellt von der Universität Kyoto
Zitat: Verfeinerung der turbulenten Strömung zur Steigerung der iPS-zellbasierten Blutplättchenherstellung (21. Juni 2024), abgerufen am 21. Juni 2024 von https://phys.org/news/2024-06-refining-turbulent-scale-ips-cell.html
Dieses Dokument unterliegt dem Urheberrecht. Mit Ausnahme der fairen Nutzung für private Studien- oder Forschungszwecke darf kein Teil ohne schriftliche Genehmigung reproduziert werden. Der Inhalt dient lediglich der Information.